Indikace: Sonografická diagnostika je vysoce senzitivní ale velmi nespecifická. Senzitivita ovšem závisí na zkušenosti operatéra (veterinárního lékaře, který vyšetření provádí). Specificitu nálezů – ať už abnormálních či vyloučení infiltrativních onemocnění, která se nemusí prezentovat ultrasonograficky detekovatelnými změnami (například infiltrativní neoplazie, inflamatorní proces, lipidóza jater) lze zvýšit pomocí odběru vzorků.
S ohledem na možná rizika je nutné před provedením odběru zvážit, jaký vliv budou mít výsledky tohoto vyšetření pro další management pacienta. Například biopsie ledviny, která může potencionálně vést k nutné nefrektomii je u pacienta s akutní nefropatií velmi diskutabilní.
Způsoby odběru pod kontrolou sonografie:
- punkce
- ultrasonograficky vedená FNA/FNAB – tenkojehelná aspirace/ aspirační biopsie
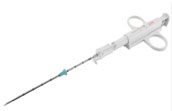
- biopsie (za použití poloautomatických či automatických systémů – např. Tru-Cut)
Punkce – cystocentéza, abdominocentéza, thorakocentéza, punkce žlučníku, punkce cystických útvarů (prostata, ledviny). Tento odběr lze provádět bez nebo s pomocí sonografie, dle preference ošetřujícího veterináře. Pod sonografickou kontrolou se jedná o techniku vhodnou jako první krok pro FNA případně biopsii, lze tak trénovat koordinaci práce rukou a navádění sonografem. Sem by případně patřila i perikardiocentéza, která se dá provádět bez nebo s kontrolou sona.
FNA je metoda ve srovnání s biopsii jednodušší, rychlejší a ve většině případů nevyžaduje sedaci/ anestezii pacienta. Je spojená s výrazně menším množstvím komplikací a dle zkušeností autorky i tyto rizika zůstávají spíše na úrovni teorie. Zpracování aspirátu je časově kratší než zpracování bioptického vzorku na histologické vyšetření, ovšem diagnostická hodnota je oproti histologii omezená.
Osobně používám obvykle 5-ml stříkačku naplněnou asi 1-2 ml vzduchu s černou jehlou, neaspiruji, pouze pohybuji jehlou v odebíraném objektu. U sleziny volím případně i tenší jehlu, u procesů kde tento postup nevede odběru materiálu zkusím aspirovat, nebo volím tlustší jehlu nebo o bojí.
Tru-cut biopsie je metoda, kde je paušálně stanovujeme koagulační parametry před zákrokem a ten pak provádíme v krátkodobé anestezii. Při zákroku v kraniální části dutiny břišní, případně hrudníku je vhodná intubace pro kontrolu dýchání resp. pohybu v inkriminované oblasti.
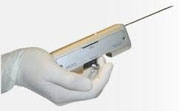
V případě abnormálních koagulačních parametrů doporučujeme terapii pacienta vitaminem K a kontrolu koagulace za týden. Provádí se buď automatickým nebo semi-automatickým systémem, volba je na osobní preferenci operatéra. Osobně používám Tru-cut systém, automatický, s možností nastavení dvou různých hladin penetrace (15 versus 22 mm) a dvě různé tloušťky jednorázových jehel: 16 a 18G (viz snímky dole a automatický systém Tru-cut vlevo).
Orgánové systémy a způsob odběru vzorků:
Játra:
- FNA – vhodná procedura u koček; dobrá senzitivita pro diagnostiku vakuolární hepatopatie a infiltrativní neoplazie; problematická detekce inflamatorních procesů.
- Biopsie – vhodná pro diagnostiku inflamatorních procesů a mikrovaskulární dysplazie
- Punkce žlučníku – pro odběr vzorku pro cytologické, případně bakteriologické vyšetření
kontraindikovaná u pacientů s mukocéle
pro riziko prosakování žluči doporučeno provedení s trojcestným ventilem a aspirace maximálního množství žluči
Slezina:
- FNA – u infiltrativních procesů možná, riziko kontaminace vzorků a nesprávná diagnóza
- biopsie
Poznámka: v případě abnormálního nálezu, zejména u fokálních lézí s ohledem na nacionále, kliniku a další nálezy lze zvážit kontrolní sonografické vyšetření za 1 – 3 měsíce, případně provést splenektomii.
Ledviny:
- FNA – u infiltrativních procesů, potvrzení suspektního renálního lymfomu (typický USG obraz)
- Biopsie – provádí se biopsie kůry. biopsie dřeně je indikovaná zřídka a je spojená s velkým rizikem poškození cév a krvácení; diagnostický vzorek by měl obsahovat minimálně 5 glomerulů (na velikosti záleží)
Poznámka: s ohledem na indikaci: potvrzeni protein-loosing nephropathy; diagnostika příčiny akutní nefropatie, nefrotický syndrom bez systemických příznaků je ovšem kritická otázka, zda je biopsie ledviny (s možným rizikem krvácení respektive ztráty ledviny) opravdu nutná a její rizika akceptovatelná. - Punkce: renálních cyst, případně s aplikací alkoholu ledvinové pánvičky: pro získání primární moči, pro aplikaci kontrastní látky
Nadledvinky:
1. + 2. FNA/Biopsie – nedoporučitelné. U feochromocytomu i u Cushingova syndromu lze diagnózu získat vyšetřením krve či moči; FNA v případě feochromocytomu může
vést k fatální hypertenzi. Navíc lokalizace nadledvinek vedle velkých cév není pro punkci či biopsii optimální.
Močový měchýř:
- Punkce – cystocentéza. Pozor u pacientů s obstrukcí močové trubice !
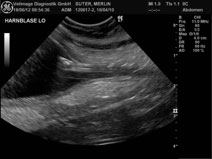
Poznámka: Cystocentézu NELZE doporučit jako techniku pro odstranění tlaku přeplněného močového měchýře s ohledem na riziko ruptury. U karcinomu přechodného epitelu je známé riziko rozsevu metastáz podél injekčního traktu. - Traumatická katetrizace – sedace, pod kontrolou sona možný cílený odběr z oblastí změn, vysoká diagnostická senzitivita cytologických vzorků pro detekci TCC (viz snímek vpravo).
Prostata:
- FNA
- Biopsie – pro oba postupy je dle klinických příznaků vhodná analgezie/sedace
Děloha, Vaječníky:
- Ovariohysterektomie
Poznámka: riziko krvácení či prosakování abnormálního obsahu dělohy do dutiny břišní je příliš vysoké a z diagnostického hlediska spíše neospraveditelné. Proto bych doporučila po revizi celé dutiny břišní (staging při podezření na neoplastický proces) přímo explorativní laparotomii.
Abdominální mízní uzliny:
- FNA – +/- sedace s ohledem na lokalizaci vedle velkých cév v případě sublumbálních mízních uzlin; biopsie možná – FNA obvykle diagnostická.
Pankreas:
- FNA: +/- sedace (pankreatické patologie jsou obvykle bolestivé)ů obvykle diagnostická i pro karcinom slinivky (u psů)
- Biopsie: ? riziko prosakování agresivních substancí slinivky a fokální peritonitidy, u cystických mas omezená diagnostická hodnota FNA/biopsie
- Explorativní laparotomie
Trávicí trakt:
- FNA – obvykle nediagnostická; doporučitelné kombinovat s FNA regionálních mízních uzlin (zejména jsou-li změněné)
- Biopsie – příliš velké riziko perforace
- Explorativní laparotomie – zároveň řeší subileus/ileus, v případě neoplazií se jedná pouze o diagnostický, případně paliativní zákrok, velmi zřídka kurativní.
Ostatní:
Podkožní a kožní útvary:
- FNA
- Biopsie
- Chirurgická excizePoznámka: sonografie může pomoci diagnostikovat lipomy, u výrazně prokrvených mas lze zúžit diferenciální diagnózu, případně se pokusit eliminovat punkci cév a kontaminaci vzorku.
Perianální oblast:
- FNA
- Biopsie
- Chirurgická excizePoznámka: týká se například análních a perianálních žláz, vaginálních mas. Sonografická vizualizace není vždy snadná. I FNA v této oblasti je pro pacienta relativně nepříjemná až bolestivá -> analgezie, sedace.
Dutina hrudní:
- FNA
- Biopsie
- CT a CT-vedený odběr vzorků
Poznámka: pro vizualizaci i odběr vzorků v oblasti hrudníku lze pracovat s polohováním pacienta, případně použít i kardiologický stůl: dependentní část plic ztrácí vzdušnost a zjednodušuje “ventrální” přístup. Vyšetřit a vzorky odebrat lze z hrudní stěny, ze sternálních mízních uzlin (drénují i kraniální část dutiny břišní !) a z periferních patologií plicního parenchymu.
Oblast krku:
- FNA – první krok prakticky za všech okolností
- Biopsie
Poznámka: jedná se obvykle o patologie v oblasti hrtanu (včetně abscesů, cizích těles) či štítné žlázy. Sedace je doporučitelná už pro samotné vyšetření, při dorzální poloze sedovaného (= velmi kooperativního) pacienta je daleko snazší orientace a rovnou možnost FNA. U biopsií pozor, masy v oblasti krku bývají bohatě krvené a rády krvácí.
Rizika:
FNA:
- kontaminace (krví)
- nediagnostický vzorek (- krvácení – FNA se nedoporučuje u pacientů s počtem trombocytů pod 30.000/ul (hranice spontánního krvácení).
- rozsev metastáz; známý z TCC popsaný i u plicních tumorů
- ruptura distendovaného močového měchýře při obstrukci močové trubice
- pneumothorax při punkci dutiny hrudní – obvykle samolimitující a vyskytující se v menší či větší míře prakticky vždy při punkci hrudníku, obvykle klinicky nedetekovatelnýBiopsie:
- krvácení
- nediagnostický vzorek – málo pravděpodobné
- pneumotorax u biopsií hrudních mas – viz FNA
- lacerace větších cév s následnou explorativní laparotomií/torakotomií, případně nefrektomií…
- popsaná fatální vagotonie jako důsledek biopsie těžce změněných jater u koček
Poznámka: jedná se o tento článek “High Complication Rate of an Automatic Tru-Cut Biopsy Gun Device for Liver Biopsy in Cats; S.J.M. Proot and J. Rothuizen; J Vet Intern Med 2006;20:1327–
1333”. Osobně jsem se s touto komplikací (zatím) nesetkala. Při zjevných změnách jater u koček provádím FNA pro vyloučení neoplastického procesu případně lipidózy. Zejména u koček je diskutabilní, nakolik biopsie v případě akutní fáze hepatopatie ovlivní další terapeutický postup.
Závěr:
FNA se dá provést téměř kdykoliv, bez větší náročnosti. Pro provedení biopsie je nutná obsáhlejší příprava a u jakéhokoliv zákroku je nutné zhodnotit nakolik jeho výsledky ovlivní další terapeutický postup pro pacienta a zda jsou rizika provedení jakékoliv invazivní diagnostiky akceptovatelné s ohledem na očekávané výsledky.
Autor:
MVDr Marta Schmidhalter Pekárková DECVDI
UK-VET sro, Evropská 677/150
160 00 Praha 6
Česká Republika
Mail: marta.pekarkova@uk-vet.cz